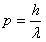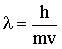โครงสร้างอะตอมตามทฤษฎีของโบร์มีลักษณธของระดับพลังงานเป็นชั้นๆ สามารถใช้อธิบายเมื่ออะตอมอยู่โดเดี่ยว หรืออะตอมอยู่ในสถานะแก๊ส
เมื่ออะตอมอยู่ชิดกันจนเปลี่ยนสถานะแก๊สเป็นของแข็ง พลังงานในอะตอมจะเปลี่ยนลักษณะไปเป็น แถบพลังงาน ที่เป็นเช่นนี้เพราะระดับพลังงานของอะตอมอยู่ชิดกันจนซ้อนทับกัน ลักษณะของแถบพลังงานมี3ส่วนคือ แถบวาเลนซ์ แถบว่าง และแถบนำไฟฟ้า ทฤษฎีแถบพลังงานนนี้สามารถอธิบายตัวนำ กึ่งตัวนะ และฉนวนได้
ก. ระดับพลังงานในของแข็ง
ข. ระดับพลังงานในอะตอมเดี่ยว
รูป 19.53 เปรียบเทียบระดับพลังงานของของแข็ง และอะตอมเดี่ยว
ในกรณีของธาตุอะตอมเดี่ยว เช่น แก๊สไฮโดรเจน (เป็นแก๊สที่อุณหภูมิ
ตัวนำ (conductor) จะมีอิเล็กตรอนเต็มในแถบวาเลนซ์ และมีอิเล็กตรอนอยู่บ้างในแถบนำไฟฟ้า เมื่อให้สนามไฟฟ้าก็จะเกิดการนำไฟฟ้าขึ้น
ฉนวน (insulator) จะมีอิเล็กตรอนเต็มในแถบวาเลนซ์ และไม่มีอิเล็กตรอนอยู่ในแถบนำไฟฟ้า มีช่องว่างระหว่างแถบพลังงาน (energy gap) ทั้งสอง ช่องว่างนี้จะกว้างมากจนเมื่อให้พลังงานไฟฟ้า(ในรูปของศักย์ไฟฟ้า) หรือพลังงานความร้อน หรือพลังงานแสง ก็ไม่สามารถทำให้อิเล็กตรอนในชั้นแถบวาเลนซ์ ถูกกระตุ้นขึ้นมาที่แถบนำไฟฟ้า จึงไม่มีการนำไฟฟ้า
<b>กึ่งตัวนำ (semiconductor) จะมีอิเล็กตรอนเต็มแถบวาเลนซ์คล้ายฉนวน แต่มีช่องว่างพลังงานเหนือแถบนั้นค่อนข้างแคบ ที่อุณหภูมิปกติ พลังงานความร้อน สามารถกระตุ้นให้อิเล็กตรอนเหล่านี้เองที่เป็นพาหะ (carrier) ของไฟฟ้าและทำให้นำไฟฟ้าได้บ้าง ทำให้ความต้านทานไม่สูงมากนักและนับเป็นสารกลุ่มกึ่งตัวนำ สารกึ่งตัวนำบางชนิดสามารกระตุ้นอิเล็กตรอนจากแถบวาเลนซ์ให้ขึ้นไปแถบนำไฟฟ้าได้ด้วยแสง และสามารถนำมาใช้เป็นประเภทLDR (Light Dependent Resistance) หรือเป็นตัวรับรู้ (sensor) แสง
ในทางปฏิบัติจะมีการใช้ฉนวน เช่น ยาง พลาสติก ทำที่หุ้มสายไฟฟ้าที่ทำจากโลหะซึ่งเป็นตัวนำไฟฟ้า ส่วนตัวต้านทานที่ใช้ในวงจรไฟฟ้าและวงจรอิเล็กทรอนิกส์นั้นจะมีค่าความต้านทานไฟฟ้าอยู่ระหว่างตัวนำกับฉนวน คือมีค่าตั้งแต่ 1 โอห์ม ถึง 100 เมกะโอห์ม